《(淮安專版)2020中考化學(xué)復(fù)習(xí)方案 專項(xiàng)11 中和反應(yīng)及探究試題》由會(huì)員分享����,可在線閱讀,更多相關(guān)《(淮安專版)2020中考化學(xué)復(fù)習(xí)方案 專項(xiàng)11 中和反應(yīng)及探究試題(5頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�。
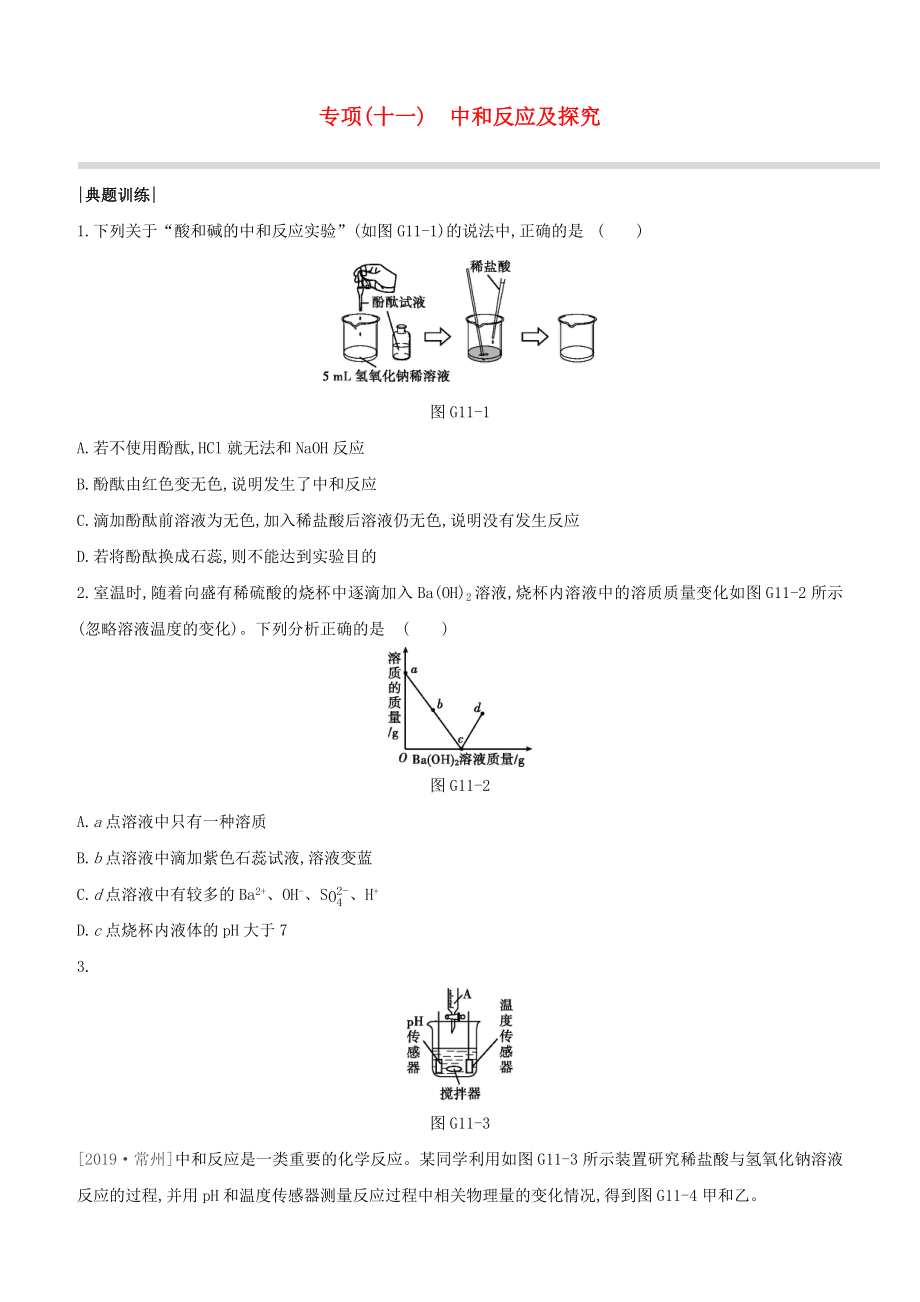
1、專項(xiàng)(十一)中和反應(yīng)及探究|典題訓(xùn)練|1.下列關(guān)于“酸和堿的中和反應(yīng)實(shí)驗(yàn)”(如圖G11-1)的說(shuō)法中,正確的是()圖G11-1A.若不使用酚酞,HCl就無(wú)法和NaOH反應(yīng)B.酚酞由紅色變無(wú)色,說(shuō)明發(fā)生了中和反應(yīng)C.滴加酚酞前溶液為無(wú)色,加入稀鹽酸后溶液仍無(wú)色,說(shuō)明沒(méi)有發(fā)生反應(yīng)D.若將酚酞換成石蕊,則不能達(dá)到實(shí)驗(yàn)?zāi)康?.室溫時(shí),隨著向盛有稀硫酸的燒杯中逐滴加入Ba(OH)2溶液,燒杯內(nèi)溶液中的溶質(zhì)質(zhì)量變化如圖G11-2所示(忽略溶液溫度的變化)��。下列分析正確的是()圖G11-2A.a點(diǎn)溶液中只有一種溶質(zhì)B.b點(diǎn)溶液中滴加紫色石蕊試液,溶液變藍(lán)C.d點(diǎn)溶液中有較多的Ba2+、OH-��、SO42-�、H
2�����、+D.c點(diǎn)燒杯內(nèi)液體的pH大于73.圖G11-32019常州中和反應(yīng)是一類重要的化學(xué)反應(yīng)�����。某同學(xué)利用如圖G11-3所示裝置研究稀鹽酸與氫氧化鈉溶液反應(yīng)的過(guò)程,并用pH和溫度傳感器測(cè)量反應(yīng)過(guò)程中相關(guān)物理量的變化情況,得到圖G11-4甲和乙�。圖G11-4(1)燒杯中發(fā)生反應(yīng)的化學(xué)方程式為。(2)儀器A中溶液的溶質(zhì)是(填化學(xué)式)���。(3)乙中V的數(shù)值最接近(填“6”“12”或“16”)�。(4)下列說(shuō)法錯(cuò)誤的是(填字母)�����。A.圖甲中b點(diǎn)所示溶液中的溶質(zhì)是NaCl和NaOHB.取圖甲中d點(diǎn)所示溶液加熱蒸干所得固體為純凈物C.圖甲中cd所示溶液中NaCl的質(zhì)量不斷增加D.圖乙中ef變化趨勢(shì)可說(shuō)明該反應(yīng)是放熱
3���、反應(yīng)4.探究酸和堿能否發(fā)生反應(yīng)方案1:甲同學(xué)向盛有少量NaOH溶液的試管中滴幾滴無(wú)色酚酞試液,振蕩,繼續(xù)加入稀硫酸,觀察到溶液由色變成無(wú)色�����。甲同學(xué)得出結(jié)論:酸和堿能發(fā)生反應(yīng)����。方案2:乙同學(xué)取少量NaOH溶液,測(cè)得溶液pH為10,向該溶液中加入一定量稀硫酸后,測(cè)得溶液pH為9。乙同學(xué)發(fā)現(xiàn)溶液pH減小了,得出結(jié)論:酸和堿能發(fā)生反應(yīng)��。交流討論:大家同意甲同學(xué)的結(jié)論,對(duì)乙同學(xué)的實(shí)驗(yàn)過(guò)程提出質(zhì)疑,溶液pH減小的原因還可能是稀硫酸中的水稀釋了NaOH溶液;大家認(rèn)為,乙同學(xué)向NaOH溶液中加入稀硫酸后,測(cè)得溶液的pH必須(填“小于”或“小于或等于”)7才能證明酸和堿能發(fā)生反應(yīng)����。5.2019雅安某化學(xué)興趣小組
4、用實(shí)驗(yàn)室常用藥品(或溶液)對(duì)“NaOH溶液與稀鹽酸是否恰好完全反應(yīng)”進(jìn)行探究����。知識(shí)卡片 氯化鈉溶液顯中性;氯化銅易溶于水。實(shí)驗(yàn)探究 (1)方案:某同學(xué)先向試管中加入約2 mL NaOH溶液,再滴入幾滴酚酞試液,溶液變紅,然后慢慢滴入稀鹽酸,邊滴邊振蕩,直至溶液恰好變?yōu)闊o(wú)色�。實(shí)驗(yàn)結(jié)論: 。從微觀的角度分析,該反應(yīng)的實(shí)質(zhì)是 �����。在滴入稀鹽酸的過(guò)程中,若觀察到有少量氣泡出現(xiàn),請(qǐng)分析產(chǎn)生氣泡的可能原因:(用化學(xué)方程式表示)�。(2)方案實(shí)驗(yàn)步驟實(shí)驗(yàn)現(xiàn)象結(jié)論取2 mL NaOH溶液于試管中,滴入一定量的稀鹽酸,振蕩后加入鎂條若 稀鹽酸過(guò)量若沒(méi)有明顯現(xiàn)象NaOH溶液與稀鹽酸恰好完全反應(yīng)實(shí)驗(yàn)反思 (3)另有同學(xué)
5、提出方案不能證明NaOH溶液與稀鹽酸恰好完全反應(yīng),其原因是���。(4)除以上方案外,下列哪些物質(zhì)單獨(dú)使用,也能證明“NaOH溶液與稀鹽酸是否恰好完全反應(yīng)”(填字母)����。A.銅片B.pH試紙C.氧化銅D.紫色石蕊試液【參考答案】1.B2.A解析a點(diǎn)時(shí),反應(yīng)沒(méi)有開(kāi)始,溶液中只有一種溶質(zhì)H2SO4,故A正確;稀硫酸與Ba(OH)2反應(yīng)生成硫酸鋇沉淀和水,溶質(zhì)質(zhì)量減小,b點(diǎn)溶液中有硫酸,滴加紫色石蕊試液,溶液變紅,故B錯(cuò)誤;完全反應(yīng)后繼續(xù)加Ba(OH)2溶液到d點(diǎn),d點(diǎn)溶液中有較多的Ba2+、OH-,無(wú)SO42-���、H+,故C錯(cuò)誤;稀硫酸與Ba(OH)2反應(yīng)生成硫酸鋇沉淀和水,溶質(zhì)質(zhì)量減小,完全反應(yīng)時(shí),溶質(zhì)質(zhì)
6、量為0,c點(diǎn)恰好完全反應(yīng),燒杯內(nèi)液體的pH=7��。3.(1)NaOH+HClNaCl+H2O(2)HCl(3)12(4)C解析(1)燒杯中發(fā)生的反應(yīng)是氫氧化鈉與稀鹽酸反應(yīng)生成氯化鈉和水,反應(yīng)的化學(xué)方程式為NaOH+HClNaCl+H2O�。(2)從反應(yīng)的pH變化圖像可知,一開(kāi)始溶液的pH大于7,故呈堿性,因此燒杯中為氫氧化鈉溶液,儀器A中為稀鹽酸,溶質(zhì)為氯化氫,化學(xué)式為HCl。(3)從圖乙中可以看出,當(dāng)體積為V時(shí)溫度不再升高,也就是兩者剛好完全反應(yīng),此時(shí)溶液的pH為7,從圖甲可以判斷出此時(shí)鹽酸的體積為12 mL��。(4)從圖甲可以看出b點(diǎn)時(shí)燒杯中的溶液pH大于7,故溶液中的溶質(zhì)為生成的氯化鈉和過(guò)量的
7���、氫氧化鈉;圖甲中d點(diǎn)時(shí)鹽酸過(guò)量,溶液中的溶質(zhì)為生成的氯化鈉和過(guò)量的氯化氫,加熱蒸干,因?yàn)辂}酸具有揮發(fā)性,氯化氫氣體會(huì)逸散到空氣中,剩余固體只含有氯化鈉,為純凈物;圖甲中c點(diǎn)時(shí),溶液的pH等于7,呈中性,此時(shí)兩種物質(zhì)恰好完全反應(yīng),再向燒杯中滴加稀鹽酸,溶質(zhì)氯化鈉的質(zhì)量不再增加;圖乙中ef的溫度逐漸升高是因?yàn)辂}酸和氫氧化鈉溶液的反應(yīng)是放熱反應(yīng)���。4.方案1:紅方案2:小于或等于5.(1)NaOH溶液與稀鹽酸恰好完全反應(yīng)H+和OH-反應(yīng)生成水分子(或H+OH-H2O)2NaOH+CO2Na2CO3+H2O,Na2CO3+2HCl2NaCl+CO2+H2O(2)有氣泡產(chǎn)生(3)稀鹽酸量不足的情況下,也無(wú)
8、明顯現(xiàn)象(4)BD解析(1)在滴入酚酞試液的試管中逐滴加入稀鹽酸,當(dāng)溶液由紅色恰好變?yōu)闊o(wú)色時(shí),說(shuō)明NaOH溶液與稀鹽酸恰好完全反應(yīng);從微觀角度看,酸堿反應(yīng)的實(shí)質(zhì)是酸中的H+和堿中的OH-反應(yīng)生成水分子;NaOH溶液易吸收空氣中的CO2生成Na2CO3,加入稀鹽酸后,會(huì)生成二氧化碳?xì)怏w而觀察到有少量氣泡產(chǎn)生��。(2)當(dāng)稀鹽酸過(guò)量時(shí),加入鎂條能與之反應(yīng)生成氫氣,則會(huì)看到有氣泡產(chǎn)生�。(3)當(dāng)稀鹽酸的量不足時(shí),加入鎂條也沒(méi)有明顯的實(shí)驗(yàn)現(xiàn)象,所以該方案不能證明NaOH溶液與稀鹽酸恰好完全反應(yīng)。(4)銅片與NaOH溶液和稀鹽酸均不反應(yīng),無(wú)法證明NaOH溶液或稀鹽酸有剩余;pH試紙�、紫色石蕊試液遇NaOH溶液和稀鹽酸會(huì)呈現(xiàn)不同顏色,可說(shuō)明反應(yīng)后的溶液是呈酸性還是堿性,以此判斷是否恰好完全反應(yīng);氧化銅能與稀鹽酸發(fā)生反應(yīng),若NaOH溶液與稀鹽酸恰好完全反應(yīng),則加入氧化銅無(wú)明顯現(xiàn)象,但當(dāng)稀鹽酸的量不足時(shí),加入氧化銅也無(wú)明顯現(xiàn)象,無(wú)法判斷是否恰好完全反應(yīng)��。
 (淮安專版)2020中考化學(xué)復(fù)習(xí)方案 專項(xiàng)11 中和反應(yīng)及探究試題
(淮安專版)2020中考化學(xué)復(fù)習(xí)方案 專項(xiàng)11 中和反應(yīng)及探究試題