《2022年高中化學《第二節(jié) 化學計量在實驗中的應用》《氣體摩爾體積》優(yōu)質(zhì)學案2 新人教版必修1》由會員分享�����,可在線閱讀���,更多相關(guān)《2022年高中化學《第二節(jié) 化學計量在實驗中的應用》《氣體摩爾體積》優(yōu)質(zhì)學案2 新人教版必修1(3頁珍藏版)》請在裝配圖網(wǎng)上搜索。
1����、2022年高中化學《第二節(jié) 化學計量在實驗中的應用》《氣體摩爾體積》優(yōu)質(zhì)學案2 新人教版必修1
【預習指導】
一、復習回顧上節(jié)課講過的公式:
二��、利用質(zhì)量���、體積、密度的關(guān)系求出體積�����,填好表中空格:
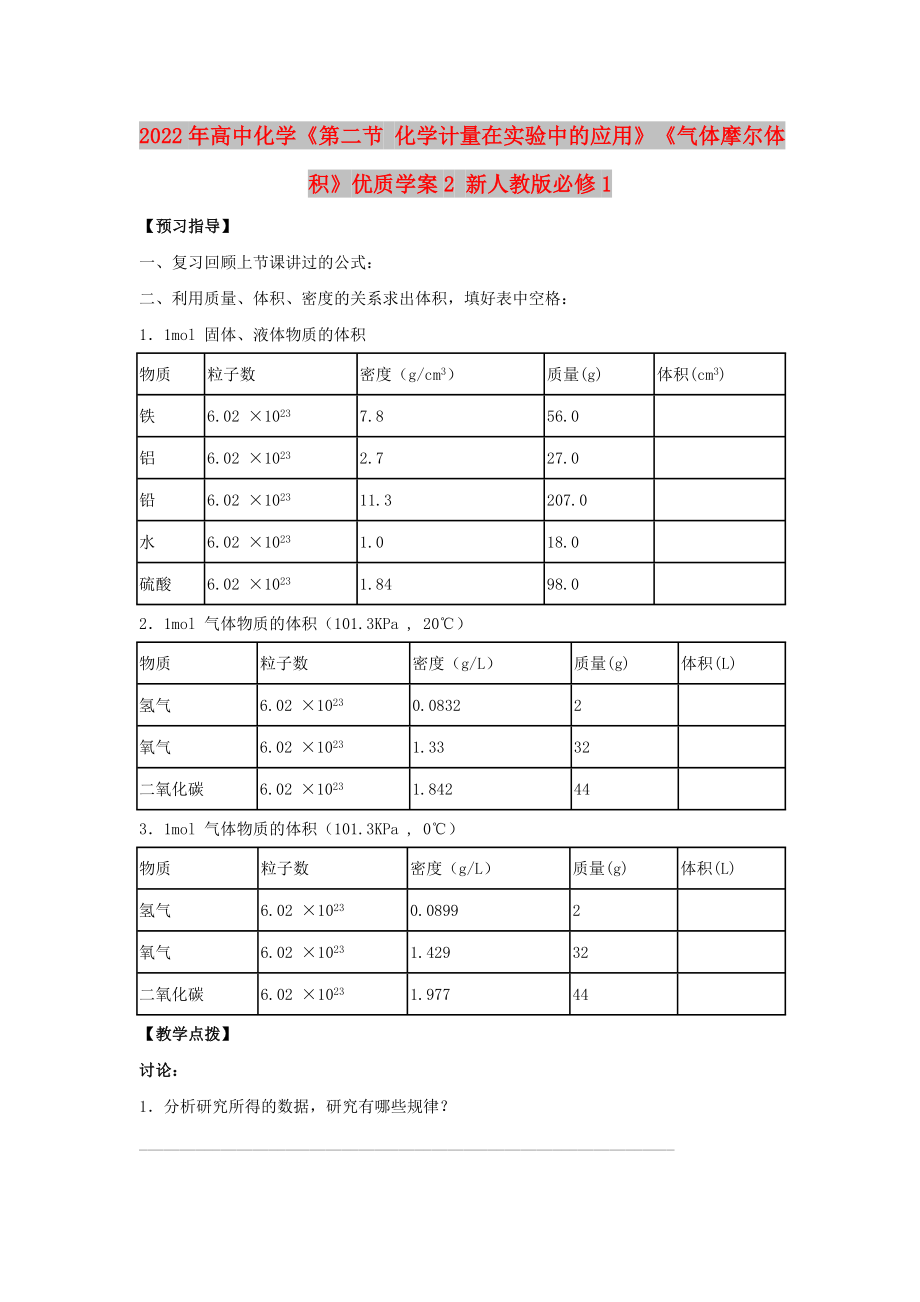
1.1mol 固體��、液體物質(zhì)的體積
物質(zhì)
粒子數(shù)
密度(g/cm3)
質(zhì)量(g)
體積(cm3)
鐵
6.02 ×1023
7.8
56.0
?
鋁
6.02 ×1023
2.7
27.0
?
鉛
6.02 ×1023
11.3
207.0
?
水
6.02 ×1023
1.0
18.0
?
硫酸
6.02 ×1023
1.84
98
2、.0
?
2.1mol 氣體物質(zhì)的體積(101.3KPa , 20℃)
物質(zhì)
粒子數(shù)
密度(g/L)
質(zhì)量(g)
體積(L)
氫氣
6.02 ×1023
0.0832
2
?
氧氣
6.02 ×1023
1.33
32
?
二氧化碳
6.02 ×1023
1.842
44
?
3.1mol 氣體物質(zhì)的體積(101.3KPa , 0℃)
物質(zhì)
粒子數(shù)
密度(g/L)
質(zhì)量(g)
體積(L)
氫氣
6.02 ×1023
0.0899
2
?
氧氣
6.02 ×1023
1.429
32
?
二氧化碳
6.02 ×102
3���、3
1.977
44
?
【教學點撥】
討論:
1.分析研究所得的數(shù)據(jù)�,研究有哪些規(guī)律�����?
__________________________________________________________________
4.是不是在相同條件下,1mol任何氣體的體積都相同呢?如何理解“任何氣體”四個字����?在其他條件下,氣體是否也遵循這些規(guī)律呢�����? __________________________________________________________________
5.充分討論總結(jié)后將下列表格補充完善:(注:影響大的用 “+”表示, 影響小的用 “-”表
4��、示)
什么是標準狀況���?為了研究方便�,我們一般只研究標準狀況下的氣體摩爾體積��,它與氣體摩爾體積的關(guān)系是什么?想象一下22.4L有多大?
【訓練反饋】
三���、練習:下列說法是否正確,為什么?
1.在標況下����,1 mol任何物質(zhì)的體積約是22.4L
2.在標況下�����,1molH2O的體積約是22.4L
3.1mol氖氣和1 mol 氧氣體積相同
4.1mol任何氣體只有在標況下才是22.4L
5.標況下��,CO2氣體摩爾體積是22.4L
6.標準狀況下��,1mol氧氣和1 mol 氮氣混合氣體(任意比)的體積約為22.4 L
7.22.4L氣體所含的分子數(shù)一定大于11.2L氣體所含的分子數(shù)
四�����、口算
?�。?)標況下����,0.5molH2占有的體積是________
?�。?)標況下����,2molO2占有的體積是________L
?����。?)標況下�����,4.48LCO2的物質(zhì)的量是________mol
?。?)標況下�,33.6LH2的物質(zhì)的量是________mol
(5)標況下�,16gO2 的體積為________L
(6)標況下����,11.2LN2 中含有N2分子的個數(shù)是________
?
 2022年高中化學《第二節(jié) 化學計量在實驗中的應用》《氣體摩爾體積》優(yōu)質(zhì)學案2 新人教版必修1
2022年高中化學《第二節(jié) 化學計量在實驗中的應用》《氣體摩爾體積》優(yōu)質(zhì)學案2 新人教版必修1