《精修版九年級(jí)化學(xué)上冊(cè) 4.2 化學(xué)反應(yīng)中的質(zhì)量關(guān)系教案 滬教版》由會(huì)員分享��,可在線閱讀�����,更多相關(guān)《精修版九年級(jí)化學(xué)上冊(cè) 4.2 化學(xué)反應(yīng)中的質(zhì)量關(guān)系教案 滬教版(2頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�。
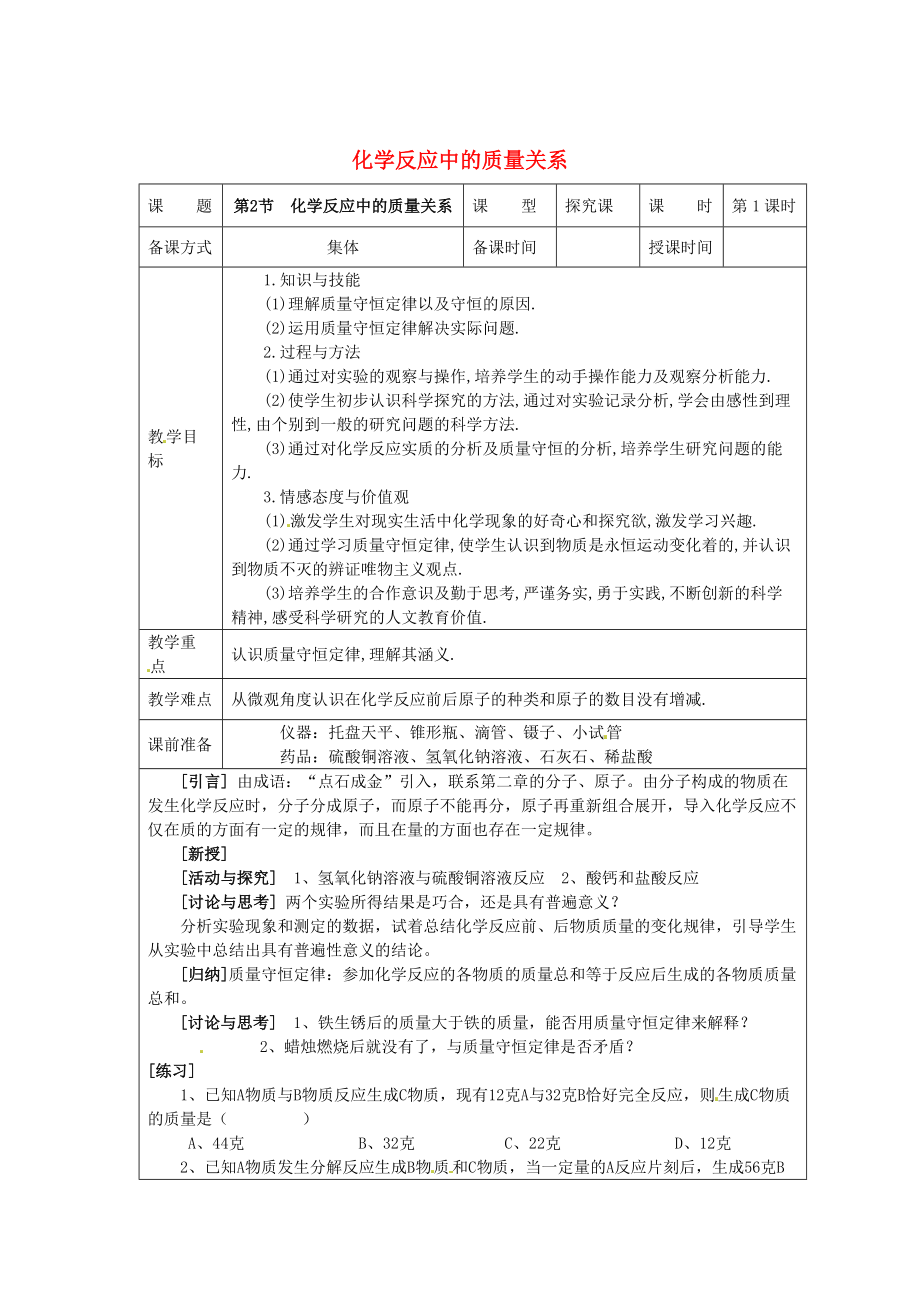
1、 精品資料化學(xué)反應(yīng)中的質(zhì)量關(guān)系課 題第2節(jié) 化學(xué)反應(yīng)中的質(zhì)量關(guān)系課 型探究課課 時(shí)第1課時(shí)備課方式集體備課時(shí)間授課時(shí)間教學(xué)目標(biāo)1.知識(shí)與技能(1)理解質(zhì)量守恒定律以及守恒的原因.(2)運(yùn)用質(zhì)量守恒定律解決實(shí)際問(wèn)題.2.過(guò)程與方法(1)通過(guò)對(duì)實(shí)驗(yàn)的觀察與操作,培養(yǎng)學(xué)生的動(dòng)手操作能力及觀察分析能力.(2)使學(xué)生初步認(rèn)識(shí)科學(xué)探究的方法,通過(guò)對(duì)實(shí)驗(yàn)記錄分析,學(xué)會(huì)由感性到理性,由個(gè)別到一般的研究問(wèn)題的科學(xué)方法.(3)通過(guò)對(duì)化學(xué)反應(yīng)實(shí)質(zhì)的分析及質(zhì)量守恒的分析,培養(yǎng)學(xué)生研究問(wèn)題的能力.3.情感態(tài)度與價(jià)值觀(1)激發(fā)學(xué)生對(duì)現(xiàn)實(shí)生活中化學(xué)現(xiàn)象的好奇心和探究欲,激發(fā)學(xué)習(xí)興趣.(2)通過(guò)學(xué)習(xí)質(zhì)量守恒定律,使學(xué)生認(rèn)識(shí)
2�����、到物質(zhì)是永恒運(yùn)動(dòng)變化著的,并認(rèn)識(shí)到物質(zhì)不滅的辨證唯物主義觀點(diǎn).(3)培養(yǎng)學(xué)生的合作意識(shí)及勤于思考,嚴(yán)謹(jǐn)務(wù)實(shí),勇于實(shí)踐,不斷創(chuàng)新的科學(xué)精神,感受科學(xué)研究的人文教育價(jià)值.教學(xué)重點(diǎn)認(rèn)識(shí)質(zhì)量守恒定律,理解其涵義.教學(xué)難點(diǎn)從微觀角度認(rèn)識(shí)在化學(xué)反應(yīng)前后原子的種類(lèi)和原子的數(shù)目沒(méi)有增減.課前準(zhǔn)備儀器:托盤(pán)天平、錐形瓶�����、滴管����、鑷子、小試管藥品:硫酸銅溶液�、氫氧化鈉溶液、石灰石��、稀鹽酸 引言 由成語(yǔ):“點(diǎn)石成金”引入�,聯(lián)系第二章的分子��、原子����。由分子構(gòu)成的物質(zhì)在發(fā)生化學(xué)反應(yīng)時(shí),分子分成原子���,而原子不能再分��,原子再重新組合展開(kāi)�,導(dǎo)入化學(xué)反應(yīng)不僅在質(zhì)的方面有一定的規(guī)律,而且在量的方面也存在一定規(guī)律���。新授活動(dòng)與探究 1��、
3����、氫氧化鈉溶液與硫酸銅溶液反應(yīng) 2����、酸鈣和鹽酸反應(yīng)討論與思考 兩個(gè)實(shí)驗(yàn)所得結(jié)果是巧合,還是具有普遍意義��?分析實(shí)驗(yàn)現(xiàn)象和測(cè)定的數(shù)據(jù)�����,試著總結(jié)化學(xué)反應(yīng)前�、后物質(zhì)質(zhì)量的變化規(guī)律,引導(dǎo)學(xué)生從實(shí)驗(yàn)中總結(jié)出具有普遍性意義的結(jié)論���。歸納質(zhì)量守恒定律:參加化學(xué)反應(yīng)的各物質(zhì)的質(zhì)量總和等于反應(yīng)后生成的各物質(zhì)質(zhì)量總和��。討論與思考 1�����、鐵生銹后的質(zhì)量大于鐵的質(zhì)量����,能否用質(zhì)量守恒定律來(lái)解釋?zhuān)?2、蠟燭燃燒后就沒(méi)有了���,與質(zhì)量守恒定律是否矛盾�?練習(xí) 1�����、已知A物質(zhì)與B物質(zhì)反應(yīng)生成C物質(zhì)�����,現(xiàn)有12克A與32克B恰好完全反應(yīng)���,則生成C物質(zhì)的質(zhì)量是( )A、44克 B���、32克 C��、22克 D��、12克 2�、已知A物質(zhì)發(fā)生分解反應(yīng)生成B
4、物質(zhì)和C物質(zhì)��,當(dāng)一定量的A反應(yīng)片刻后��,生成56克B和44克C��;則實(shí)際發(fā)生分解的A物質(zhì)的質(zhì)量為( )A���、12克 B�、44克 C���、56克 D����、100克 3����、關(guān)于質(zhì)量守恒定律,下列敘述中正確的是( )A、煤燃燒化為灰燼�����,該反應(yīng)不符合質(zhì)量守恒定律B���、24克鎂在空氣中完全燃燒生成40克氧化鎂��,實(shí)際消耗空氣的質(zhì)量為16克C����、一切化學(xué)反應(yīng)都遵守質(zhì)量守恒定律D����、質(zhì)量守恒定律只適用于有氣體或固體生成的化學(xué)反應(yīng)指導(dǎo)學(xué)生畫(huà)重點(diǎn)講解:參加反常反應(yīng)的各物質(zhì)質(zhì)量總和的“總和”二字是指真正參加化學(xué)反應(yīng)的各物質(zhì)(有的反應(yīng)并未全部參加反應(yīng)) 反應(yīng)物、生成物的質(zhì)量應(yīng)包括氣體����、沉淀等全部物質(zhì)的質(zhì)量 審題時(shí)要注意關(guān)鍵的字,如“充分反
5����、應(yīng)”“恰好反應(yīng)”“足量反應(yīng)”等表示的意義�。講座與思考 為什么“質(zhì)量守恒定律”能夠成立?投影 水分解示意圖���、碳和氧氣在化全生成二氧化碳的示意圖學(xué)生分析化學(xué)變化的微觀實(shí)質(zhì)�����,指導(dǎo)學(xué)生看書(shū)���,引導(dǎo)學(xué)生分析質(zhì)量守恒的原因板書(shū):“質(zhì)量守恒定律”成立的原因 原子的種類(lèi)��、原子的個(gè)數(shù)�、原子的質(zhì)量都不發(fā)生改變練習(xí)1��、蠟燭燃燒后的產(chǎn)物有二氧化碳和水�����,由質(zhì)量守恒定律可知��,石蠟的組成中一定含有 �、 �、 元素2、根據(jù)質(zhì)量守恒定律:在A2 +B2= 2C 中����,“C”的化學(xué)式用A��、B可表示 ��。本節(jié)小結(jié)1�、質(zhì)量守恒定律的內(nèi)容;2���、用微觀的觀點(diǎn)理解質(zhì)量守恒定律���。布置作業(yè):1、已知2克氫氣與16克氧氣恰好完全反應(yīng)��,生成水的質(zhì)量為 克2�����、已知A與B反應(yīng)生成C和D�,(A+B=C+D),現(xiàn)有80克A與一定量的B恰好完全反應(yīng)����,生成124克C和36克D,則參加反應(yīng)的B的質(zhì)量為 克3���、某物質(zhì)在氧氣中燃燒只生成二氧化碳�����,則該物質(zhì)的組成中一定含有 元素4���、在4X +5Y2 =2Z2的反應(yīng)中,Z的化學(xué)式用X�����、Y表示為( )A�、X4Y5 B、X2Y5 C�、XY2 D、X4Y10教后記
 精修版九年級(jí)化學(xué)上冊(cè) 4.2 化學(xué)反應(yīng)中的質(zhì)量關(guān)系教案 滬教版
精修版九年級(jí)化學(xué)上冊(cè) 4.2 化學(xué)反應(yīng)中的質(zhì)量關(guān)系教案 滬教版