《中考命題研究(遵義)2020中考化學 教材知識梳理 第4章 認識化學變化 課時2 化學反應中的質量關系 化學方程式(無答案)》由會員分享�,可在線閱讀,更多相關《中考命題研究(遵義)2020中考化學 教材知識梳理 第4章 認識化學變化 課時2 化學反應中的質量關系 化學方程式(無答案)(7頁珍藏版)》請在裝配圖網(wǎng)上搜索�����。
1�����、課時2化學反應中的質量關系化學方程式五年中考命題規(guī)律年份題型題號涉及內容分值2020選擇題8�����、5.D質量守恒定律22填空題15.方案(一)(1)���、18方案(二)(1)化學方程式的書寫�,根據(jù)化學方程式的計算242020選擇題8.AD���、9質量守恒定律�����,書寫化學方程式及計算22填空����、計算題16.方案3、17根據(jù)化學方程式的計算152020選擇題10根據(jù)化學方程式的計算2填空題12.(2)����、14.(4)�、15(2)(3)、17���、18質量守恒定律�,利用化學方程式的簡單計算214552020填空題13.(1)(2)�����、14.(3)���、18質量守恒定律�,利用化學方程式的簡單計算2242020選擇題7質量守恒定律
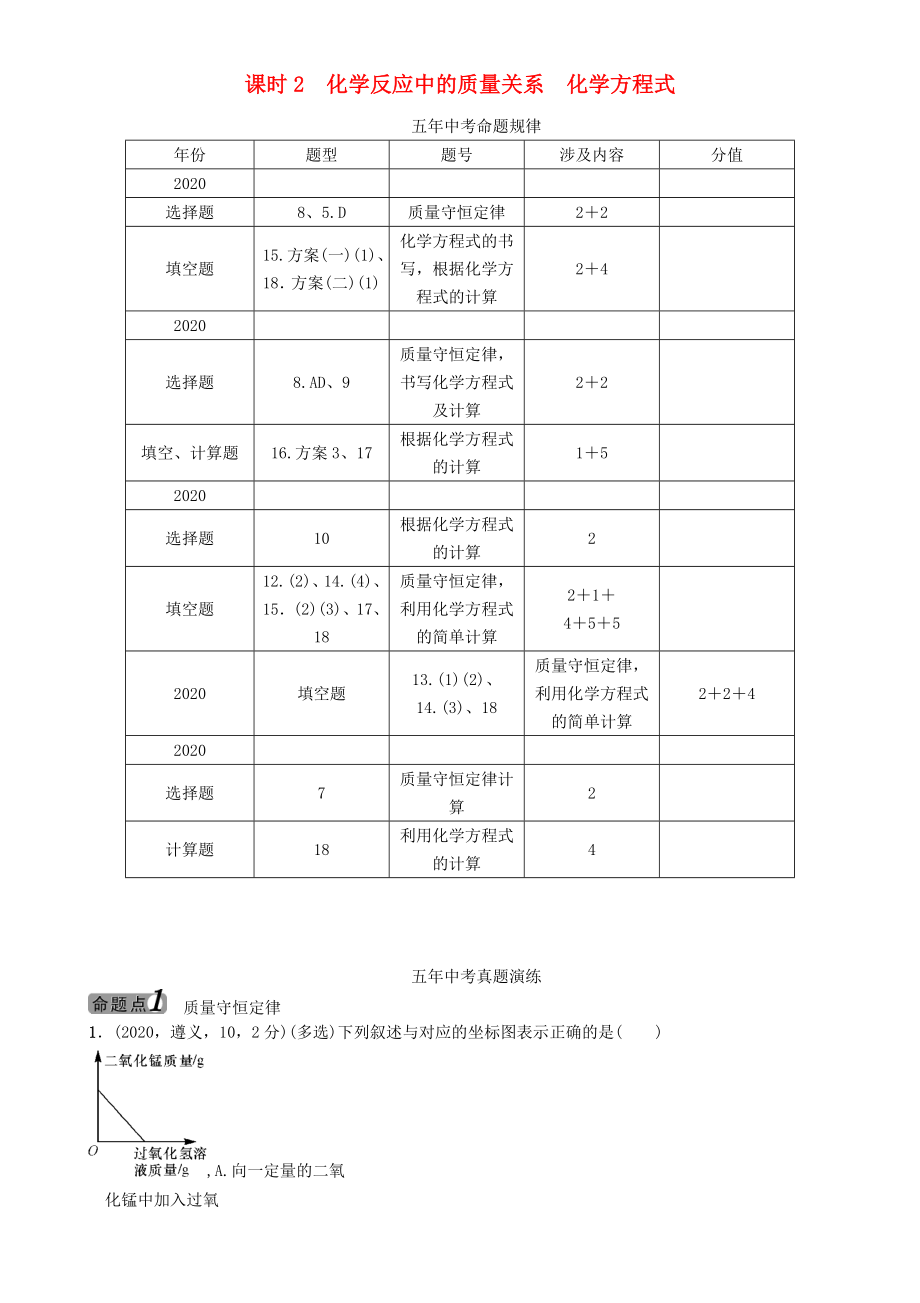
2��、計算2計算題18利用化學方程式的計算4五年中考真題演練質量守恒定律1(2020�����,遵義,10����,2分)(多選)下列敘述與對應的坐標圖表示正確的是(),A.向一定量的二氧化錳中加入過氧化氫溶液,B.將相同質量的Zn粉和Mg粉分別加入足量的稀鹽酸中,C.在一定量AgNO3和Cu(NO3)2的混合溶液中加入鐵粉 ,D.加熱一定量的高錳酸鉀固體2(2020,遵義���,7���,2分)在一密閉容器中有X、Y����、Z、W四種物質����,在一定條件下充分反應,測得反應前后各物質的質量如下表所示�。下列說法中正確的是()物質XYZW反應前質量/g810121反應后質量/g021待測9A.反應后Z的質量為9 gB反應中Y與W發(fā)生改變的質
3、量比為11C反應生成Y的質量為11 gDZ在該反應中作催化劑3(2020�����,遵義,8����,2分)質量守恒定律是幫助我們認識化學反應實質的重要理論。在化學反應aAbBcCdD中����,下列說法正確的是()A化學計量數(shù)a與b之和一定等于c與d之和B若A和C都是鹽,則該反應一定是復分解反應C反應物A和B的質量比一定等于生成物C和D的質量比D若取x g A和x g B反應�����,生成C和D的質量總和不一定是2x g化學反應的表示方法4(2020����,遵義����,9,2分)下列應用和相應的原理(用化學方程式表示)及基本反應類型都正確的是()A用熟石灰制生石灰CaOH2OCa(OH)2化合反應B用氯酸鉀和二氧化錳制氧氣2KClO3M
4�、nO2,2KCl3O2分解反應C用天然氣作燃料CH42O2點燃CO22H2O氧化反應D用純堿制燒堿2KOHNa2CO3K2CO32NaOH復分解反應52020,遵義�,12(1)(2),2分如圖是某化學反應過程的微觀模擬圖���,請結合圖示回答下列問題:(1)寫出該微觀模擬圖所表示的化學反應方程式_�。(2)根據(jù)如圖信息,從微觀角度說出化學反應的實質是_(答一條即可)��。62020����,遵義,12(2)�,1分化學用語是研究化學的工具。請按要求回答下列問題:如圖是某反應的微觀示意圖�����。該反應的化學方程式是_�。利用化學方程式的簡單計算7(2020,遵義�����,10��,2分)完全燃燒2.8 g某有機物�����,生成8.8 gCO2和
5、3.6 gH2O�����,下列對該有機物的判斷正確的是()A該有機物一定含碳���、氫�、氧元素B該有機物的化學式為CH4C該有機物的相對分子質量為46D該有機物由碳��、氫元素組成����,且碳、氫元素的質量比為618(2020���,遵義,8�,2分)下圖為某化工企業(yè)生產(chǎn)流程示意圖,有關說法正確的是()A中氬氣(Ar)作反應物B鈦酸亞鐵(FeTiO3)中鈦元素為3價C中為使原料全部轉化為甲醇�,理論上CO和H2投料的質量比為71D中反應為2FeTiO36C7Cl2一定條件2X2TiCl46CO,則X為FeCl29(2020�,遵義,18��,4分)煤是重要的化工原料,用煤做燃料不僅是極大的浪費�����,而且因煤中含有硫的化合物(如FeS2)
6����、,燃燒時生成SO2氣體��,造成對環(huán)境的污染����。有一種煤中含5%的FeS2(假設煤中除FeS2外的其他成分中不含硫元素),燃燒時���,設煤中的硫全部轉化為二氧化硫被排入大氣���,F(xiàn)eS2燃燒時的化學方程式為:4FeS211O2高溫2Fe2O38SO2,某火力發(fā)電廠燃燒3000噸這種煤���,可產(chǎn)生多少噸SO2?中考考點清單質量守恒定律1質量守恒定律���。(1)內容:_的各物質的_等于反應后生成的各物質的_��?����!咎貏e提醒】 質量守恒定律的特點反應:化學反應質量:反應物��、生成物的質量總和:反應物質量總和生成物 質量總和(2)宏觀與微觀解釋�。 五個“不變”宏觀反應物和生成物的_不變_種類不變微觀原子_不變原子_不變原子_不變
7�、兩個“一定改變”宏觀:物質的_微觀:_兩個“可能改變”_2質量守恒定律的應用。(1)解釋化學變化和生活中的一些現(xiàn)象��。(2)推斷某反應物�����、生成物的組成元素���。(3)推斷化學方程式中的未知化學式及化學式前的系數(shù)。(4)判斷化學方程式書寫是否正確���。(5)利用質量守恒定律進行簡單的計算�����。3實驗:質量守恒定律的驗證�����。(1)實驗裝置:(2)探究質量守恒定律的條件和要求�。反應物或生成物的狀態(tài)實驗要求沒有氣體參與或沒有氣體生成的反應發(fā)生化學反應,且反應現(xiàn)象明顯有氣體參與或有氣體生成的反應在密閉容器中發(fā)生化學反應�����,且反應現(xiàn)象明顯(3)現(xiàn)象分析���。發(fā)生化學反應的現(xiàn)象(說明肯定發(fā)生了化學反應)�;天平的平衡情況(說明反應
8�����、前后的質量關系)�;對天平不平衡的解釋(反應中是否有氣體生成;外界物質是否進入����;用氣球收集反應生成的氣體時浮力的影響等)。化學反應的表示方法(高頻考點)1定義:用_來表示_的式子叫化學方程式�����。2書寫原則:以_為依據(jù)����,符合_定律。3書寫步驟:,寫寫出反應物����、生成物的_,標標明化學反應的_,標出產(chǎn)物的_���,把短線改為“_”,配_化學方程式,查一查化學式是否正確二查是否配平三查生成物狀態(tài)是否標注����、標注是否恰當四查反應條件是否標明利用化學方程式的簡單計算1計算依據(jù):化學方程式中各物質間的質量關系���。2計算步驟��。煅燒100 kg的石灰石�,最多可得到氧化鈣多少千克���?分析過程按題意設未知數(shù)��;寫出題中反應的化學方程
9����、式���;找出反應物和生成物的質量關系����;建立已知量和未知量的比例關系�����;計算x����,并作答。解答格式解:設最多可得到氧化鈣的質量為xCaCO3高溫CaOCO2 100 56 100 kg x100,56100 kg,x�����,x56 kg答:最多可得到氧化鈣56 kg���。中考重難點突破推斷化學方程式中的化學式或化學式前的系數(shù)【例1】(2020�����,武漢)二氧化鈦(TiO2)是一種用途廣泛的化工原料�����。用四氯化鈦(TiCl4)與某常見物質X反應可制得二氧化鈦�����,反應的化學方程式為TiCl4XTiO24HCl����。關于物質X,下列說法正確的是()A該物質由碳�、氫、氧三種元素組成B該物質的化學式為H2O2C該物質中氫�����、氧元素的質量
10�、比為18D該物質中氫元素的質量分數(shù)是5%【解析】根據(jù)化學反應前后原子的種類與數(shù)目不變,可列表確定X的組成元素:TiOHCl生成物1244已知反應物1004差值(X)0240X由氫元素和氧元素組成����,且化學式中氫原子和氧原子的個數(shù)比為21�����,所以X的化學式為H2O,只有C正確�。【答案】C1.(2020�,遵義)“碳循環(huán)”是自然界中重要的一類物質轉化,CO2在該轉化中起著非常重要的作用�����。如圖是這種作用的具體體現(xiàn)之一�。有機物AO2CO2堿,酸無機鹽某有機物R在空氣中完全燃燒的化學方程式:R3O2點燃2CO23H2O,R的化學式為_���。判斷物質的元素組成【例2】(2020��,株洲)某物質W在空氣中完全燃燒后的產(chǎn)
11���、物只有二氧化碳和水。根據(jù)以上信息�����,下列關于物質W組成的說法中正確的是()A含有C、H�����、O三種元素B只含C����、H元素C含有C、H元素���,可能含有O元素D含有C元素��,可能含有H��、O元素【解析】化學反應前后元素種類不變��,物質W在空氣中完全燃燒后的產(chǎn)物只有二氧化碳和水��,表明W中一定含有碳元素和氫元素�,但是由于反應物中有氧氣參加�����,根據(jù)生成水和二氧化碳,無法推斷W中是否含有氧元素��?!敬鸢浮緾2.某可燃物4.6 g在足量氧氣中充分燃燒,生成8.8 g二氧化碳和5.4 g水�����,則該可燃物的組成為()A一定含碳�、氫��、氧三種元素B一定含碳��、氫元素�,可能含氧元素C一定含碳、氫元素��,不含氧元素D所含元素大于三種化學方程式的
12���、書寫【例3】(2020���,黃岡)請用所學的化學知識解釋下列現(xiàn)象。(1)一氧化碳用于煉鐵的原理(用化學方程式表示)_��。(2)用天然氣作燃料的原理(用化學方程式表示)_。(3)將一包放置較長時間的食品干燥劑放入燒杯中���,加入足量的稀鹽酸�����,可能發(fā)生反應的化學方程式是:_���、_、_(寫出三個即可)����。【解析】(1)一氧化碳與氧化鐵在高溫下生成鐵和二氧化碳���;(2)天然氣的主要成分甲烷與的氧氣在點燃條件下反應����,生成水和二氧化碳����,同時放出熱量。(3)常用來作食品干燥劑的生石灰,生石灰與水反應生成氫氧化鈣�,與鹽酸反應生成氯化鈣和水,氫氧化鈣與鹽酸反應生成氯化鈣和水�,變質生石灰中碳酸鈣與鹽酸反應生成氯化鈣、水和二氧化碳
13���、�����?!敬鸢浮?1)3COFe2O3高溫2Fe3CO2(或4COFe3O4高溫3Fe4CO2)���;(2)CH42O2點燃CO22H2O;(3)CaOH2OCa(OH)2��;CaO2HClCaCl2H2O��;2HClCa(OH)2CaCl22H2O(或CaCO32HClCaCl2H2OCO23.(2020����,遵義)九年級化學學習的物質和化學反應在日常生活中有著實際的應用。(1)氫氣被認為是最清潔的燃料����,用化學方程式解釋其原因_����。(2)鹽酸能除去鐵制品表面的鐵銹(鐵銹主要成分:Fe2O3)����,該化學反應方程式為_?;瘜W方程式的有關計算【例4】(2020,北京)利用化學反應2NaH22NaH可實現(xiàn)氫氣的存儲���,計算230 g金屬鈉最多可吸收氫氣的質量��?!敬鸢浮拷猓涸O可吸收氫氣的質量為x��。2NaH22NaH 46 2 230 g x2,46x,230 gx10 g答:230 g金屬鈉可吸收氫氣的質量為10 g��?!痉椒ㄖ笇А扛鶕?jù)化學方程式計算需要注意以下問題:(1)化學方程式是化學計算的依據(jù),因此必須書寫正確����,并且一定要配平���,因為根據(jù)未配平的化學方程式計算出來的量是不正確的;(2)根據(jù)化學反應方程式求出的質量比是純物質間的質量比�,所以代入化學方程式計算的必須是純物質的質量;(3)當題目給出量的單位不統(tǒng)一時���,一定要換算成同一單位����。
 中考命題研究(遵義)2020中考化學 教材知識梳理 第4章 認識化學變化 課時2 化學反應中的質量關系 化學方程式(無答案)
中考命題研究(遵義)2020中考化學 教材知識梳理 第4章 認識化學變化 課時2 化學反應中的質量關系 化學方程式(無答案)